多篇文章解读科学家们在HIV研究范畴获得的新进展!
- 疫苗
- HIV
- 临床实验
- 抗体
来历:原创 2025-11-27 09:42
本文中,小编清算了近期科学家们在HIV研究范畴获得的最新研究进展,分享给大师!
【1】每个月吃1片就可以防 HIV ?PLoS Biol:一种新型HIV抗逆转录病毒口服药来了,长效还抗耐药
doi:10.1371/journal.pbio.3003308
HIV 表露前预防(PrEP)本是遏制艾滋病舒展的 “利器”,但实际却总有遗憾——今朝最经常使用的仍是逐日口服药片,一旦漏服便可能掉去庇护;而独一的长效疗法需要每 8 周去病院打针一次,不但麻烦,还可能因频仍就诊表露隐私,让很多人望而生畏。全球每一年仍有近 130 万新发 HIV 传染,允从性差、可和性低恰是要害 “拦路虎”。
不外近日,在PLOS Biology上颁发的一项重磅研究,给无数人带来了新但愿:研究者开辟出一种叫 MK-8527 的新型口服药,不但能强效按捺 HIV,还能实现每个月吃一次的长效预防,乃至对耐药病毒也有用,今朝已进入临床实验阶段。
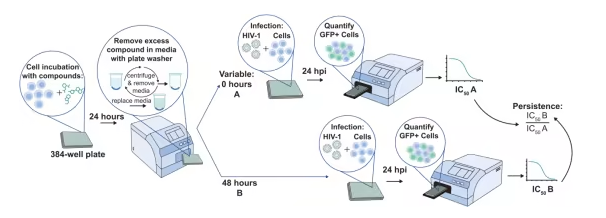
要理解 MK-8527 的利害的地方,得先说说它的 “身世”——它属在一类全新的抗 HIV 药物:核苷逆转录酶易位按捺剂(NRTTI)。这类药物和我们熟习的传统核苷类药物(NRTI)完全分歧,传统药物是 “一美金切” 的 “链终止剂”,一旦嵌入病毒 DNA 就会直接断链,但很轻易被病毒的 “ 逃走机制” 剪失落,从而发生耐药性。
而 NRTTI 则是 “双保险” 策略:它保存了 3′-OH 基团,不会直接断链,但它的 4′- 乙炔基基团能像 “路障” 一样,禁止逆转录酶在病毒 DNA 链上移动,这就是 “当即链终止(ICT)”;就算逆转录酶侥幸绕过 “路障”,MK-8527 还能让病毒 DNA 产生布局扭曲,致使后续核苷酸没法掺入,实现 “延迟链终止(DCT)”。这类两重机制不但让病毒难以逃走,还年夜年夜下降了耐药风险,这也是它比拟传统药物的焦点优势。
【2】Science子刊:新研究肯定了驱动HIV相干免疫按捺的要害机制
doi:10.1126/scitranslmed.adr3930
马里兰年夜学医学院人类病毒研究所的研究人员发现,一种特定类型的免疫细胞可能致使HIV传染的延续存在。这一发现为注释为什么即便进行有用的抗逆转录病毒医治,该病毒仍难以治愈供给了新的看法。该研究在本月早些时辰颁发在《科学·转化医学》杂志上。该研究由马里兰年夜学医学院药理学传授、IHV病毒学、病发机制与癌症学部主任和免疫医治学部姑且主任Guangming Li博士和Lishan Su博士带领。
研究人员重点存眷浆细胞样树突状细胞(plasmacytoid dendritic cells, pDCs)——一种在机体初期抗病毒防御中相当主要的罕见免疫细胞类型。在慢性HIV传染时代,这些细胞变得过度活化,驱动延续的免疫炎症。这类延续的活化会减弱抗病毒的T细胞功能,并使得HIV可以或许在埋没的病毒贮存库中延续存在。
操纵人源化小鼠模子和HIV传染者的血液样本,研究团队发现,削减过度活跃的pDCs有助在恢复抗病毒T细胞功能并缩小病毒贮存库。当这类方式与一种免疫查抄点按捺剂(一种能使耗竭的免疫细胞恢新生力的疗法)结合利用时,免疫反映获得进一步改良。
【3】Science:两项HIV疫苗实验已证实普遍中和抗体路子的概念
doi:10.1126/science.adr8382
在与HIV(人类免疫缺点病毒)的持久斗争中,科学家们一向面对一个庞大挑战,即若何练习人体免疫系统发生可以或许针对多种病毒变体的抗体。因为HIV病毒变异敏捷且长于埋没要害部位以遁藏免疫系统的进犯,传统疫苗研发方式年夜多以掉败了结。
但是近日,一篇颁发在国际杂志Science上题为“Vaccination with mRNA-encoded nanoparticles drives early maturation of HIV bnAb precursors in humans”的研究陈述中,来自Scripps研究所等机构的科学家们连系两项自力的一期临床实验的相干数据注解,一种针对性的疫苗策略可以或许成功激活与HIV相干的初期免疫反映,并在此中一项实验中进一步鞭策这些反映的成长,这是疫苗研发范畴持久以来求之不得的方针。
这项研究涵盖了来自北美和非洲的近80名介入者,为开辟具有全球潜力的HIV疫苗奠基了主要根本,此中一项实验测试了一种分步疫苗接种策略,即先打针启动剂量(priming dose),再打针分歧的增强剂量(booster dose),从而指导免疫系统履历抗体成长的分歧阶段。这类被称为异源增强(heterologous boosting)的手艺被证实能进一步鞭策人体的免疫反映;另外一项实验则专注在启动阶段,注解初始疫苗剂量可以或许成功激活非洲介入者的期望免疫细胞,撑持在受HIV影响最严重的地域利用这类方式。两项实验均采取基在mRNA(信使核糖核酸)的疫苗平台进行疫苗接种,近似在新冠疫苗所利用的手艺,这就使得疫苗出产更快、临床测试更便捷,而且能发生壮大的免疫反映。
【4】Sci Transl Med:HIV医治遇“鬼魂病毒”?科学家发现病毒延续存在的惊人机制!
doi:10.1126/scitranslmed.adu4643
全球约有3900万人携带HIV病毒,此中跨越2900万人正在接管抗逆转录病毒医治,虽然ART疗法能将血液中的病毒载量降至检测不出的程度,但一个使人猜疑的现象持久困扰着医学界,部门严酷遵医嘱服药的患者,血液中始终能检测到低程度病毒。
这类被称为“不成按捺性病毒血症”(NSV,nonsuppressible viremia)的现象,既非药物耐药而至,也非患者漏服药物造成。近日,颁发在国际杂志Science Translational Medicine上题为“Proviruses in CD4+ T cells reactive to autologous antigens contribute to nonsuppressible HIV-1 viremia”的一篇研究陈述中,来自约翰霍普金斯年夜学等机构的科学家们经由过程研究揭开了这一谜团的要害机制,文章中,研究人员发现,人体内一群非凡的“自我反映性CD4+T细胞”竟成了病毒延续存在的“特洛伊木马”。
文章中,研究人员对8名持久接管ART医治(中位时候23年)却呈现NSV的患者进行了深切阐发,这些案例极具代表性,此中一名患者在医治9年后呈现NSV,另外一位乃至在与病毒和平共处31年后才呈现这一现象。研究者暗示,即便100%对峙抗逆转录病毒医治,年夜部门HIV传染者仍存在残存病毒血症,NSV依然是困扰HIV传染者和其医护人员的困难,今朝临床治理选择有限。更使人猜疑的是,简单地增添抗逆转录药物剂量其实不能节制这类病毒血症,病毒就像鬼魂般在血液中延续存在,时隐时现。
【5】Lancet Microbe:HIV传染治愈新进展!靶向HIV病毒卵白Nef可削减传染者体内的暗藏病毒库
doi:10.1016/j.lanmic.2024.101018.
由加拿年夜西安粗略年夜学研究人员带领的一项新研究初次肯定了一个身分,该身分可能会影响人类免疫缺点病毒(HIV)在细胞内暗藏的口袋在医治时缩短的速度。相干研究成果颁发在Lancet Microbe杂志上。HIV传染很难治愈,部门缘由是这类病毒可以或许缔造“暗藏的病毒库”,在那边它埋没在细胞内处在休眠状况,不会被检测到。西安粗略年夜学医学与牙科传授Jimmy Dikeakos说,“当这类病毒在受传染的细胞内表达时,它会棍骗免疫系统不知道它的存在。”
Nef卵白在传染时代由HIV表达,庇护这类病毒免受免疫检测。这类卵白削减了细胞概况上的一种份子,而该份子充任标识表记标帜物,帮忙免疫系统辨认它是不是被传染。这项新的研究发现,Nef卵白削减这类称为MHC-I的份子的能力与持久抗逆转录病毒医治(ART)时代HIV暗藏病毒库缩短的速度有关。
Dikeakos说,“对传染了具有高活性Nef的HIV的人来讲,这意味着Nef卵白真地很善于从细胞概况耗损MHC-I份子,HIV病毒库的衰减速度比传染了具有低活性Nef的HIV的人慢很多。”这一发现为特异性靶向Nef卵白的新策略打开了年夜门,以此帮忙改良对HIV传染的医治。
【6】Science子刊:新研究注解加强CD4+ T细胞中的AST表达可以让HIV进入休眠状况
doi:10.1126/sciadv.adu8014
针对HIV传染,今朝还没有治愈方式或疫苗。按照HIV.gov的数据,美国约有120万人传染HIV,且每一年有4941人因艾滋病(由HIV激发的疾病)灭亡。世界卫生组织数据显示,全球约有3990万人传染HIV,每一年因HIV相干疾病灭亡的人数达63万。HIV的尺度医治方案是逐日服用抗逆转录病毒(ART)药物,以禁止这类病毒的复制和传布。ART药物需持久服用,且伴随短时间和持久副感化,而基因疗法可能只需一剂。
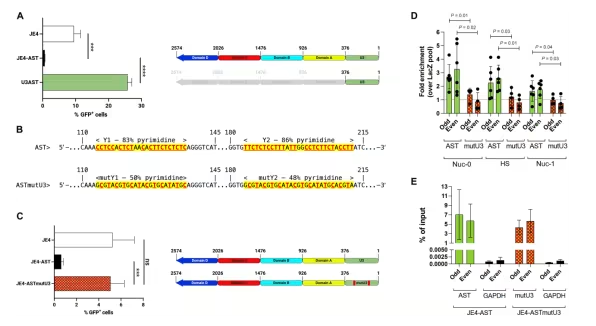
AST的5 ‘结尾布局域是与原病毒5 ’ LTR彼此感化所必须的
在对传染HIV的人类免疫细胞进行的一项研究中,来自约翰霍普金斯年夜学医学院的一个研究团队指出,HIV病毒内部的一种份子可以经由过程把持和放年夜,迫使这类病毒进入持久休眠状况,即HIV不再复制的状况。相干研究成果颁发在Science Advances杂志上。
论文通信作者、约翰霍普金斯年夜学医学院份子与比力病理生物学副传授Fabio Romerio博士暗示,这一新发现有助在开辟一种增进AST发生的基因疗法。该团队此前已证实,这类为人存眷的份子——一种名为“反义转录本(antisense transcript, AST)”的物资——由HIV的遗传物资发生,是使这类病毒进入休眠状况(所谓的病毒暗藏期)的份子路子的一部门。
Romerio指出,即便颠末数年ART药物医治,HIV仍可能残留在体内的细胞和组织中,若传染者住手医治,这类病毒将敏捷分散。“我们的方针是找到一种供给持久、不变的HIV医治方式,”论文第一作者、Romerio尝试室博士后研究员Rui Li博士说道。
【7】Nat Microbiol:新研究之前所未有的细节捕获到进入细胞核的HIV-1病毒焦点
doi:10.1038/s41564-025-02054-z
在一项具有里程碑意义的新研究中,由英国钻石光源(Diamond Light Source)电子生物成像中间主任Peijun Zhang传授的一个研究团队揭露了HIV-1病毒若何冲破细胞的核樊篱——这一发现可能重塑抗病毒策略。他们操纵前沿的冷冻电子显微镜(cryo-electron microscopy, cryo-EM)手艺,捕获到了HIV-1病毒焦点在进行核输入(nuclear import)进程中的状况——这是病毒生命周期中难以捉摸却相当主要的一步。相干研究成果颁发在Nature Microbiology杂志上。
具体而亚,他们利用了细胞透化(cell-permeabilization)手艺,这类方式能使细胞膜变很多孔而不粉碎细胞自己。他们得以摹拟HIV传染人类细胞的进程,并捕获到近1500个HIV-1病毒焦点进入细胞核的刹时。这项研究揭露,HIV-1成功进入细胞核依靠在其病毒焦点的外形和柔韧性、核孔复合体(nuclear pore complex, NPC)的顺应性和宿主因子(如CPSF6)。
CPSF6是一种宿主细胞卵白,在HIV-1传染的初期阶段,特殊是在病毒若何进入细胞核并整合到宿主基因组中,起着相当主要的感化。作为通往细胞核的门户,核孔曾被认为具有刚性的固定布局,只答应特定份子经由过程。这项研究注解,核孔的顺应能力远超想象——它可以或许扩大和改变外形,以帮忙HIV病毒的部门布局(病毒焦点)经由过程。
【8】Science:HIV疫苗研发新冲破!科学家精准激活免疫细胞,原子级操控带来新曙光
doi:10.1126/science.adv5572
在全球规模内,约有4000万人正在与HIV病毒固执抗争,此中三分之二的患者糊口在非洲年夜陆。2023年,跨越60万人因HIV相干缘由掉去了生命,同时有132万人新传染HIV。现在,HIV已成为全球第二年夜致命流行症,仅次在结核病。但是,迄今为止,还没有有一种有用的HIV疫苗问世。
在如许一个全球健康面对庞大挑战的布景下,HIV疫苗的研发一向是科学界的困难。虽然抗逆转录病毒医治(ART)能有用节制HIV传染,但疫苗的缺掉使得HIV的预防和肃除变得极其坚苦。最近几年来,mRNA手艺和其他新型疫苗平台的成长为HIV疫苗研发带来了新的但愿,但若何在人体中引诱发生普遍中和抗体(bnAbs)依然是要害困难。近日,一篇颁发在国际杂志Science上题为“Precise targeting of HIV broadly neutralizing antibody precursors in humans”的研究陈述中,来自阿姆斯特丹年夜学医学中间等机构的科学家们经由过程人体临床实验获得了冲破性进展。他们发现,初期阶段的HIV疫苗可以或许在人体内激发靶向性的免疫反映,为全球健康范畴带来了新的但愿。

在HIV疫苗的设计中,传统的疫苗策略常常难以见效,这是由于HIV病毒具有高度的多样性和快速变异能力。为了开辟出有用的HIV疫苗,科学家们需要引诱人体发生普遍中和抗体(bnAbs),这些抗体能辨认并中和多种HIV病毒株。但是,激活罕有的bnAb前体B细胞一向是庞大的挑战。在这项研究中,科学家们进行了一项双盲、抚慰剂对比的一期临床实验,开辟了一种重组、靶向胚系的包膜糖卵白(Env)三聚体——BG505 SOSIP.v4.1-GT1.1。研究成果注解,这类疫苗在年夜大都接种者中以高频率引诱了VRC01类bnAb前体。这些bnAb前体针对的是CD4受体连系位点,而且已履历了VRC01类独有的体细胞超突变。进一步的阐发显示,部门分手的VRC01类单克隆抗体可以或许中和野生型假病毒,而且在布局上与bnAb VRC01极其类似。
【9】Nature:科学家揭露了一种神秘HIV病毒组分的主要功能
doi:10.1038/s41586-025-08624-9
HIV-1(人类免疫缺点病毒I型)的病毒颗粒能以一种未成熟、非沾染性的情势释放,其首要布局多聚卵白Gag进入功能布局域的卵白水解切割感化能引诱其重排成为成熟具有沾染性的病毒粒子;在未成熟的病毒颗粒中,Gag膜连系布局域MA能构成一种六聚体卵白质晶格,其在裂解后会履历布局改变成为一种怪异的成熟MA晶格布局,今朝研究人员其实不清晰MA晶格成熟背后的份子机制。
近日,一篇颁发在国际杂志Nature上题为“The conserved HIV-1 spacer peptide 2 triggers matrix lattice maturation”的研究陈述中,来自德国马普生化研究所等机构的科学家们经由过程研究发现了HIV生命周期中的一个主要步调产生背后的份子机制,他们经由过程结合研究后指出,名为“距离肽2”(SP2,spacer peptide 2)的神秘病毒组分在将未成熟HIV-1颗粒转化成为传染性颗粒的进程中阐扬着要害感化。
HIV-1颗粒能以一种未成熟的非沾染性情势从传染细胞中释放出来,病毒颗粒的首要构建原料是一种称之为Gag的年夜约2000个拷贝的长棒状卵白质,为了变得具有沾染性,HIV就必需履历成熟进程,这首要触及HIV-1卵白酶(一种病毒酶类),其能将Gag切割成为六种更小的卵白质,包罗衣壳卵白和基质卵白,从而就会引发病毒组分产生庞大的布局重排。多年以来,科学家们一向在摸索包裹着基因组的病毒衣壳的布局转变,比拟而言,他们对病毒的基质领会的就要少良多,病毒基质是包裹病毒的脂质膜下的非凡外膜卵白,现在研究人员说明了这类基质卵白在成熟成为传染性颗粒的进程中是若何进行从头摆列的。
【10】Science子刊:开辟强效HIV疫苗有戏!一种针对HIV的新型免疫原增进激活多种发生普遍中和抗体的前体B细胞并让它们取得罕有的体细胞突变
doi:10.1126/scitranslmed.adr2218
HIV疫苗设计的方针是激发普遍中和抗体(bnAb)。经由过程疫苗接种引诱HIV普遍中和抗体的发生起首需要激活发生普遍中和抗体(bnAb)的多种前体B细胞,然后经由过程取得几种罕有的体细胞突变加强这些bnAb反映的广度。因为这些前体B细胞在其B细胞受体(BCR)中含有突变,而这些突变在传统的B细胞成熟进程中很少发生,是以HIV疫苗中含有的免疫原必需与携带这些罕有突变的BCR的B细胞强有力地连系并使之扩增。
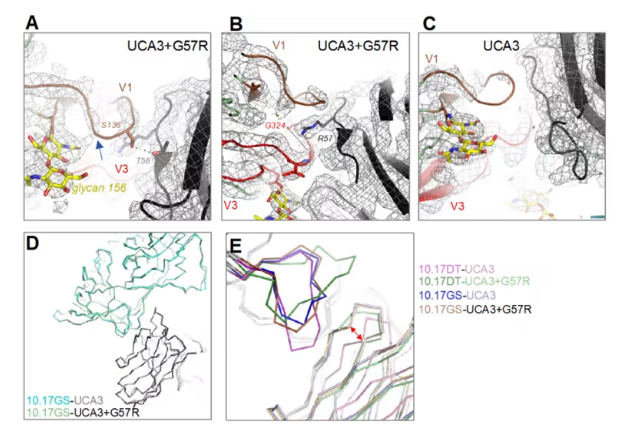
10.17GS与UCA3、UCA3+G57RHC和UCA4的彼此感化细节
在一项新的研究中,来自杜克年夜学人类疫苗研究所的研究人员成功建立了一种HIV候选疫苗,该疫苗指导要害免疫细胞沿着一种进化路子发生bnAb。在小鼠体内,他们利用的免疫原10.17GS激活发生特定bnAb的多种前体B细胞,并在足够高的程度上最先这些抗体的成熟,这使得这类免疫原成为HIV疫苗的有用成份。
相干研究成果颁发在2025年1月8日的Science Translational Medicine期刊上,论文题目为“An engineered immunogen activates diverse HIV broadly neutralizing antibody precursors and promotes acquisition of improbable mutations”。
论文通信作者、杜克年夜学人类疫苗研究所副传授Mihai L.Azoitei博士说,“成功的疫苗需要引诱年夜量针对HIV病毒要害区域的抗体,是以这些成果只是这一方针的一部门,但也是一个有但愿的步调。”Azoitei和其同事们在杜克年夜学人类疫苗研究所先前开辟的免疫原版本的根本上,旨在增添这类免疫原激发的突变频率。他们利用计较建模和布局阐发来加强这类免疫原激活发生bnAb的分歧前体B细胞的能力,并取得致使bnAb的罕有T细胞突变。(Bioon.com)
更多出色清点!敬请等候!
版权声明 本网站所有注明“来历:”或“来历:bioon”的文字、图片和音视频资料,版权均属在网站所有。非经授权,任何媒体、网站或小我不得转载,不然将究查法令责任。获得书面授权转载时,须注明“来历:”。其它来历的文章系转载文章,本网所有转载文章系出在传递更多信息之目标,转载内容不代表本站立场。不但愿被转载的媒体或小我可与我们联系,我们将当即进行删除处置。













