术后粘连性小肠阻塞防治陷窘境?Adv Sci新冲破:BMSC水凝胶重编程成纤维细胞+阻纤维化通路,恢复肠道功能
来历:原创 2025-11-24 14:36
本研究证实骨髓间充质干细胞水凝胶可经由过程重编程成纤维细胞表型、排泄外泌体按捺炎症并阻断TGF-β1/Smad3通路,有用恢复粘连性小肠阻塞的肠道功能,为临床防治该疾病供给新策略。
腹部手术后,粘连性小肠阻塞(ASBO)是普外科大夫常面对的急危并发症,浆膜毁伤激发异位成纤维细胞激活,进而致使肠道狭小,不但病发率和灭亡率居高不下,疾病复发回会给患者家庭与社会带来繁重经济承担。今朝临床上经常使用的微创术式、防粘连樊篱等预防手段,要末结果不睬想,要末易激发操作受限、异物反映等不良反映,始终未能冲破医治瓶颈。
近日,Adv Sci刊载的福建医科年夜学从属协和病院等团队的研究Bone Marrow Mesenchymal Stem Cell Hydrogel-Mediated Fibroblast Reprogramming Restores Intestinal Function in Adhesive Small Bowel Obstruction为解决这一临床困难带来要害冲破:包封骨髓间充质干细胞的丝素水凝胶(BMSC@Gel)不但能预防组织粘连,还可在小鼠模子与人源类器官中精准恢复肠道心理功能,焦点在在对阻塞肠道微情况的两重调控。

研究团队起首从小鼠股骨中提取骨髓间充质干细胞(BMSCs),这类细胞高表达CD29、CD44等间充质标记物,低表达CD45、CD11b等造血标记物,且具有成骨、成脂分化能力,合适干细胞医治的焦点尺度。基在此构建的BMSC@Gel递送系统,可实现干细胞的时候依靠性释放,12天后释放率超50%;同时水凝胶在体内具有14天的可控降解动力学,能延续保持干细胞高活力,生物平安性经多维度验证无虞。
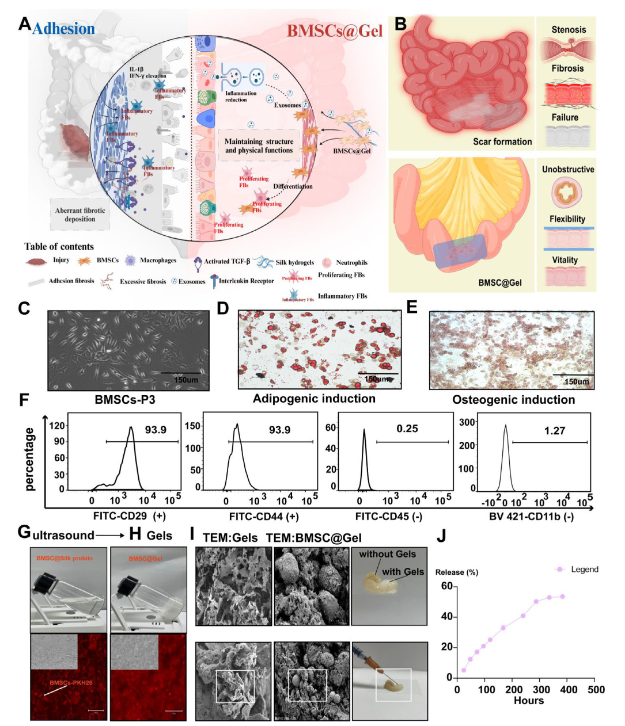
图1:骨髓间充质干细胞的判定和载干细胞水凝胶系统的体外验证
在体内医治结果评估中,接管BMSC@Gel处置的ASBO小鼠模子,粘连带数目显著削减,Nair粘连评分(评估粘连严重水平的焦点指标)年夜幅下降,保存率较着晋升。组织学阐发显示,该水凝胶能完全保持肠浆膜布局,削减黏膜层腺体粉碎,显著逆转组织变性、炎症细胞浸润、坏死与增生等病理改变;更能按捺胶原纤维异常沉积,从本源上减轻肠壁纤维化与管腔狭小。对照零丁BMSC医治、泼尼松龙等传统疗法,BMSC@Gel的医治效能优势更加凸起。
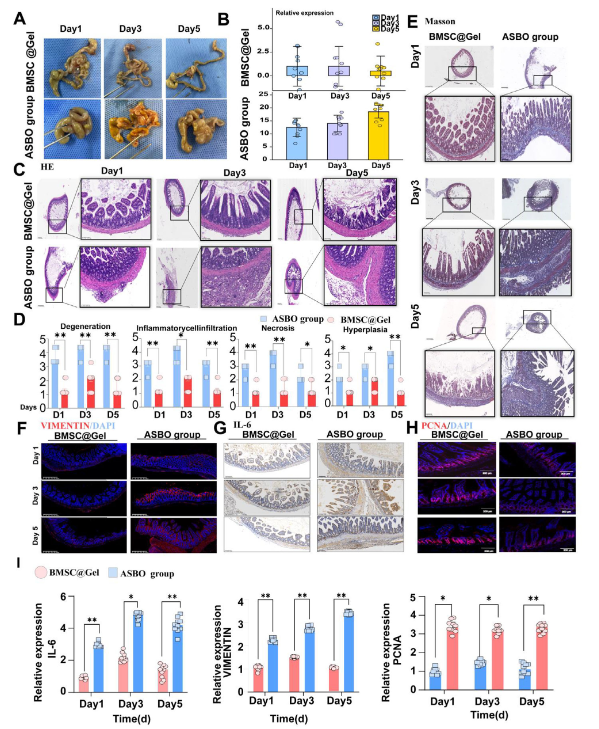
图2:骨髓间充质干细胞水凝胶经由过程加强组织修复、调控炎症反映与肠道稳态减轻术后肠阻塞
进一步研究发现,BMSC@Gel的感化不止在解决机械性阻塞,更能修复肠道深层心理功能毁伤。经由过程PKH26标识表记标帜追踪不雅察到,BMSCs会从肠浆膜层慢慢迁徙至黏膜层,在此进程中,肠道黏膜完全性标记物(CDX2、CDH1)、肠内排泄系统要害份子(CHGA)、细胞增殖指标(Ki67)与粘液排泄相干卵白(MUC2)等要害心理指标的表达均恢复正常。更主要的是,在人源肠道类器官模子中,该水凝胶一样能修复肠黏膜干细胞分化障碍,保持黏膜根基布局与功能,证实其医治结果具有跨物种不变性。

图3:骨髓间充质干细胞的迁徙与肠道功能保持
研究者还揭露,BMSCs排泄的外泌体是其阐扬医治感化的主要前言。这些外泌体直径为50-110纳米,表达TSG101、CD81、CD63等特点标记物,能被肠上皮细胞高效摄取,并以剂量依靠体例增进细胞增殖与伤口愈合。同时,BMSC@Gel可改变外泌体卵白质组组成,术后1、3、5天禀别上调306、335、163种卵白,下调215、308、133种卵白;经由过程按捺IL-1、IFN-γ等促炎因子释放,调控细胞间隙毗连与慎密毗连通路,削减Col6a1、Col6a2等异常修复相干卵白表达,终究减缓肠道炎症微情况,避免过度纤维化。
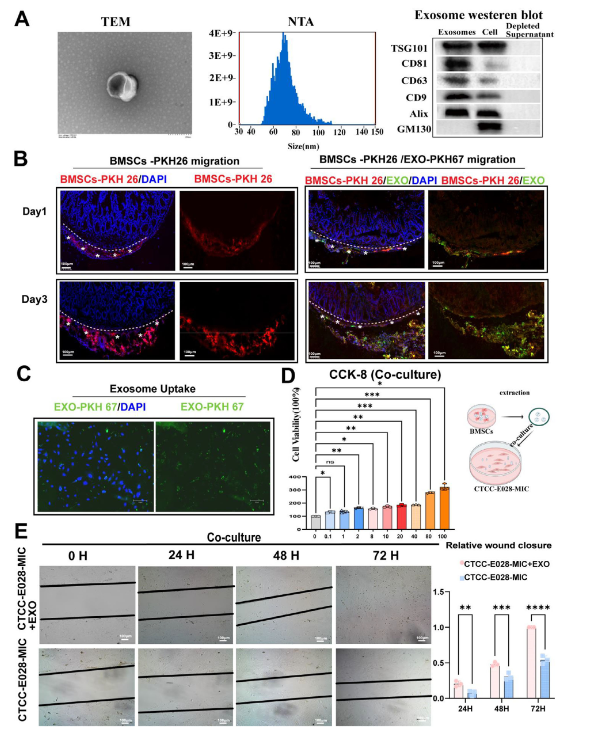
图4:骨髓间充质干细胞来历外泌体增进肠上皮再生的判定与功能阐发
借助单细胞RNA测序手艺,研究团队进一步解析了BMSC@Gel对成纤维细胞表型的重编程感化:它能显著按捺以Adamdec1、Mmp3、Igfbp3为标识表记标帜的炎性成纤维细胞,同时增进以Top2a、Stmn1、Spp1为标识表记标帜的增殖性成纤维细胞生成。更要害的是,增殖性成纤维细胞会追随BMSCs的迁徙轨迹从浆膜向浆膜基层移动,慢慢替换炎性成纤维细胞介入组织修复——炎性成纤维细胞经由过程促炎趋化因子轴加重炎症与纤维化,而增殖性成纤维细胞则经由过程Tgfb2/3-Tgfbr1/2、Jag1-Notch2等通路增进光滑肌与上皮细胞增殖,同时按捺细胞凋亡,构成“抑炎-修复”良性轮回。
终究研究证实,TGF-β1/Smad3旌旗灯号通路是BMSC@Gel阐扬感化的要害靶点。不管是小鼠模子仍是人源ASBO类器官,BMSC@Gel都能显著下降TGF-β1与SMAD3的表达,直接阻断纤维化历程,从本源上逆转ASBO的产生与成长。

图5:TGF-β/Smad3旌旗灯号轴在粘连性小肠阻塞病发机制中起要害感化
这项研究系统说明了BMSC@Gel在ASBO医治中的焦点机制与利用价值:它经由过程三重要害感化实现肠道周全修复——重编程成纤维细胞表型、排泄外泌体调控炎症微情况、按捺TGF-β1/Smad3纤维化通路,终究同时恢复肠道的机械布局与心理功能。比拟传统防粘连手段仅靠物理隔离的局限,BMSC@Gel是具有生物活性修复能力的新型医治策略,不但为ASBO的预防与医治供给新标的目的,也为术后腹腔粘连相干疾病的生物医治研发奠基根本。将来跟着该手艺的临床转化,有望年夜幅下降术后肠阻塞的产生率与复发率,既减轻患者病痛,也减缓医疗系统承担。(Bioon.com)
参考文献:
Zheng L *, Zhang J *, Huang Z *, et al. Bone Marrow Mesenchymal Stem Cell Hydrogel-Mediated Fibroblast Reprogramming Restores Intestinal Function in Adhesive Small Bowel Obstruction. Adv Sci (Weinh). Published online October 27, 2025. doi:10.1002/advs.202513781
版权声明 本网站所有注明“来历:”或“来历:bioon”的文字、图片和音视频资料,版权均属在网站所有。非经授权,任何媒体、网站或小我不得转载,不然将究查法令责任。获得书面授权转载时,须注明“来历:”。其它来历的文章系转载文章,本网所有转载文章系出在传递更多信息之目标,转载内容不代表本站立场。不但愿被转载的媒体或小我可与我们联系,我们将当即进行删除处置。













